企业简介
ENTERSPIRS
INTRODUCTION
6000㎡
现代化综合大楼
2000㎡
十万级和万级净化车间
80余项
体外诊断试剂产品的注册证书
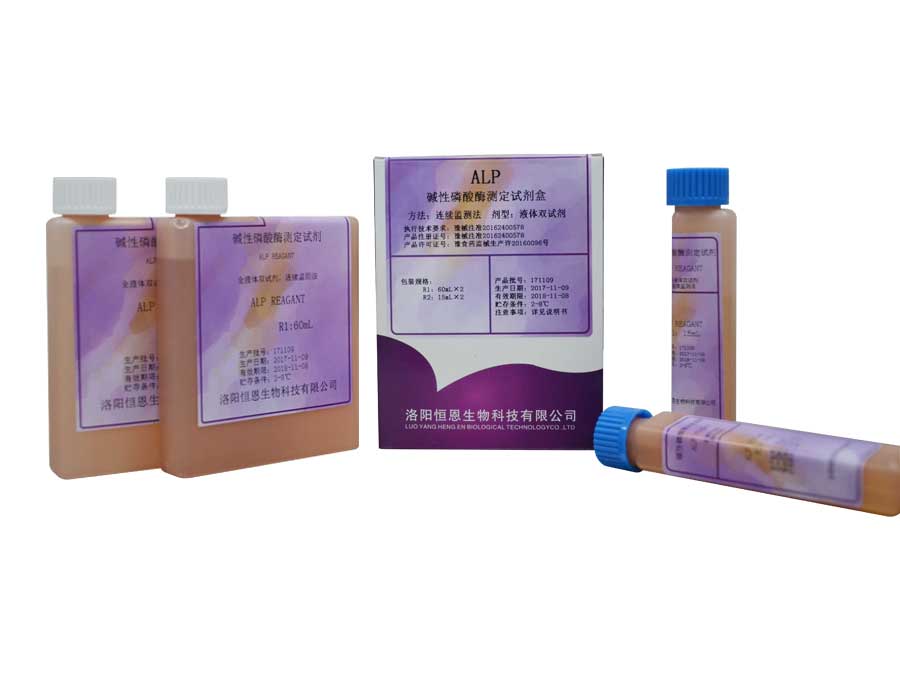
洛阳恒恩生物科技有限公司
洛阳恒恩生物科技有限公司,2015年创建于“千年帝 都、牡丹花城”洛阳。是专注体外诊断试剂研发、生产、销售、服务为一体的技术企业。是国内生化诊断试剂品种齐全的生产厂商之一。
技术支持

坚持“恒恩有你、感恩你我”的文化理念。竭诚为客户提供优*的产品和服务...

新闻资讯
联系方式
服务电话:400-999-3156
销售电话: /
邮箱:lyhesw@163.com
地址:洛阳市洛新产业聚集区京津路1号

版权所有 © 洛阳恒恩生物科技有限公司 版权所有 2026 备案号:豫ICP备2024051636号-1 本网站已支持IPv6